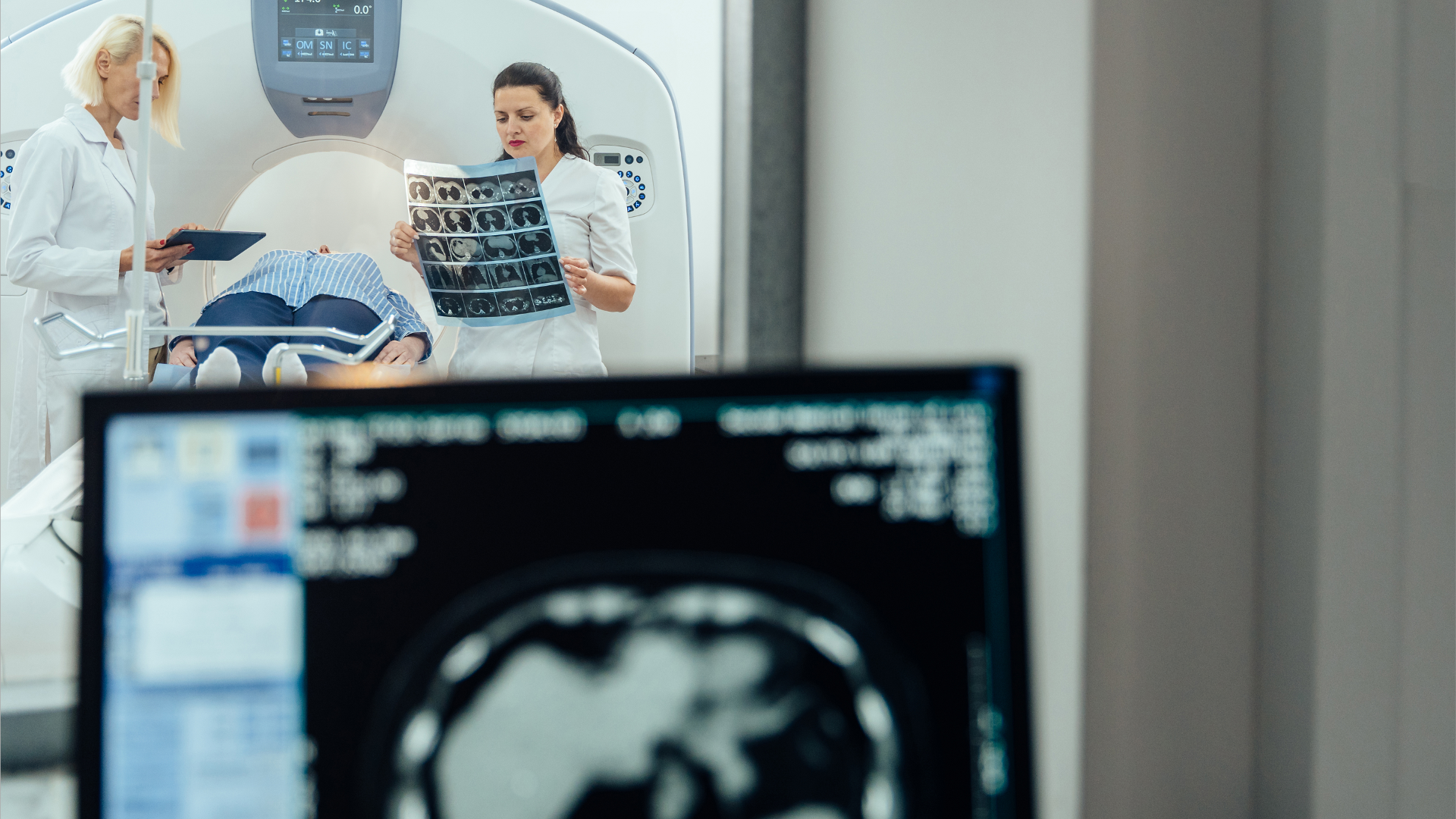
MEDIZINPRODUKTE
(MDR) Medizinprodukteverordnung
Die globale Medizinprodukteindustrie steht unter zunehmendem Druck, nicht nur Sicherheit und Qualität, sondern auch Datentransparenz, Lebenszyklusverantwortung und Nachhaltigkeit nachzuweisen .
In der EU schaffen die Medizinprodukteverordnung (EU) 2017/745 (MDR) und die In-vitro-Diagnostika-Verordnung (EU) 2017/746 (IVDR) einen neuen Rechtsrahmen dafür, wie Medizinprodukte auf dem europäischen Markt hergestellt, registriert und überwacht werden. Diese Gesetze gelten für Hersteller, Importeure, Händler und Bevollmächtigte, die Medizin- oder Diagnostikprodukte auf dem EU-Markt in Verkehr bringen - von kleinen Anbietern chirurgischer Instrumente bis hin zu großen multinationalen Produktherstellern.
Die MDR und die IVDR sollen sicherstellen, dass jedes Produkt von der Herstellung bis zur Verwendung durch den Patienten rückverfolgt werden kann, wodurch sowohl die Patientensicherheit als auch die Transparenz der Lieferkette verbessert werden.
Sie stehen auch im Zusammenhang mit den umfassenderen Nachhaltigkeitszielen im Rahmen des EU Green Deal und der Richtlinie über die Nachhaltigkeitsberichterstattung von Unternehmen (CSRD), da genaue Produktdaten für die ESG-Berichterstattung und die Verfolgung der Kreislaufwirtschaft von entscheidender Bedeutung sind.
Bei osapeers arbeiten Fachleute für Compliance und Nachhaltigkeit zusammen:
- Verstehen Sie, wie digitale Rückverfolgbarkeit und die eindeutige Gerätekennzeichnung (UDI) das Risikomanagement und die ESG-Kennzahlen verbessern.
- Erfahrungen mit der Umsetzung des regulatorischen Datenaustauschs über EUDAMED und GUDID austauschen.
- MedTech-Unternehmen, Krankenhäuser und Lieferanten in einer Gemeinschaft verbinden, die sich auf interoperable und nachhaltige Gesundheitssysteme konzentriert.