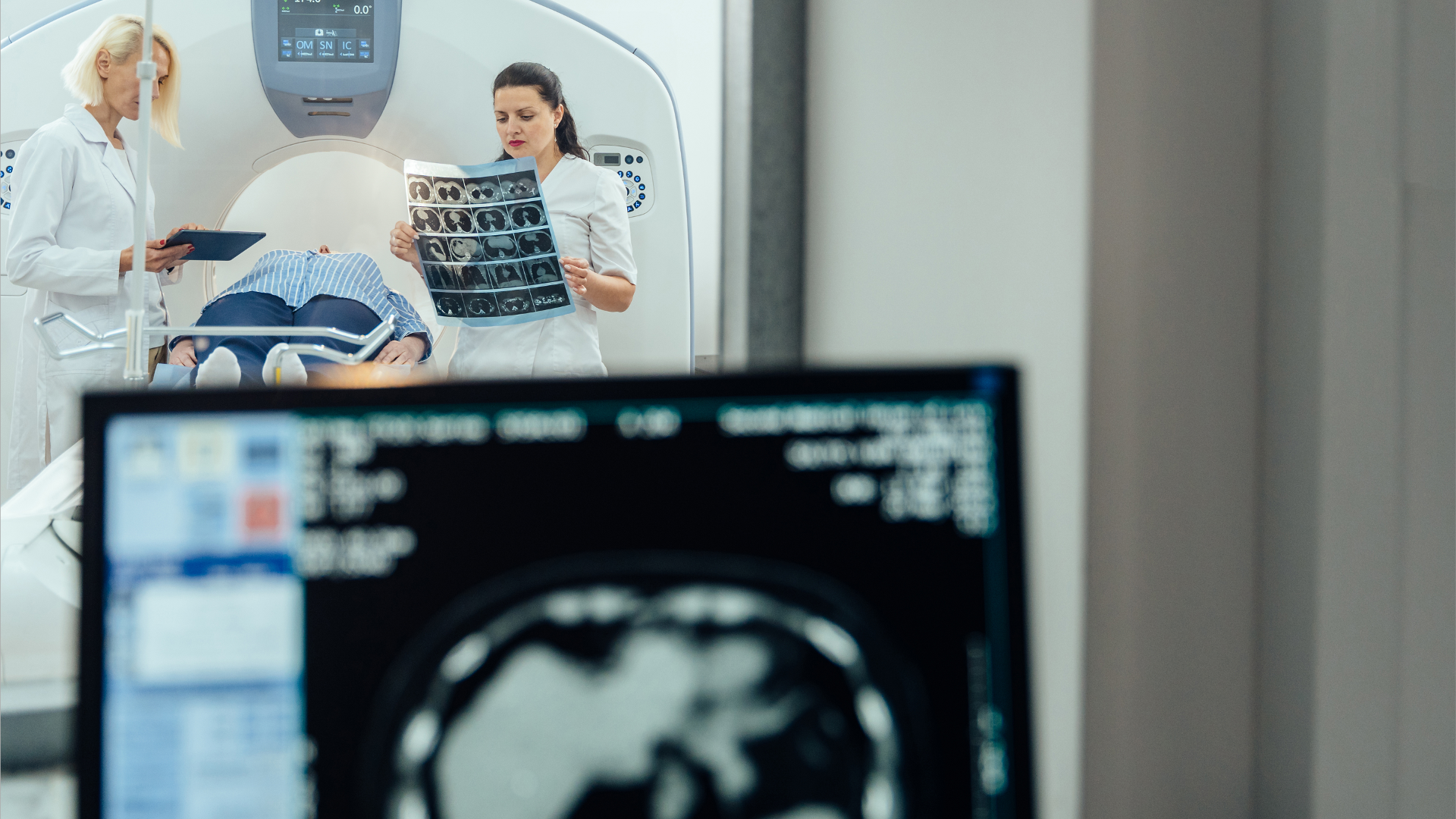
DISPOSITIVOS MÉDICOS
(MDR) Reglamento sobre productos sanitarios
La industria mundial de dispositivos médicos se enfrenta a una presión cada vez mayor para demostrar no solo seguridad y calidad, sino también transparencia de datos, responsabilidad sobre el ciclo de vida y sostenibilidad.
En la UE, el Reglamento de Productos Sanitarios (UE) 2017/745 (MDR) y el Reglamento de Diagnóstico In Vitro (UE) 2017/746 (IVDR) establecen un nuevo marco legal sobre cómo se fabrican, registran y supervisan los productos sanitarios en todo el mercado europeo. Estas leyes se aplican a fabricantes, importadores, distribuidores y representantes autorizados que comercializan productos sanitarios o de diagnóstico en el mercado de la UE, desde pequeños proveedores de instrumentos quirúrgicos hasta grandes multinacionales productoras de productos sanitarios.
El MDR y el IVDR tienen como objetivo garantizar que todos los productos puedan ser rastreados desde su producción hasta su uso por parte del paciente, reforzando tanto la seguridad del paciente como la transparencia de la cadena de suministro.
También están vinculados a objetivos de sostenibilidad más amplios en el marco del Pacto Verde de la UE y de la Directiva sobre informes de sostenibilidad corporativa (CSRD), ya que los datos precisos de los productos se convierten en fundamentales para los informes ESG y el seguimiento de la circularidad.
En osapeers, los profesionales del cumplimiento y la sostenibilidad colaboran para:
- Comprenda cómo la trazabilidad digital y la identificación única de dispositivos (UDI) mejoran la gestión de riesgos y las métricas ESG.
- Compartir experiencias en la implementación del intercambio de datos reglamentarios a través de EUDAMED y GUDID.
- Conecta a empresas de tecnología médica, hospitales y proveedores en una comunidad centrada en sistemas sanitarios interoperables y sostenibles.